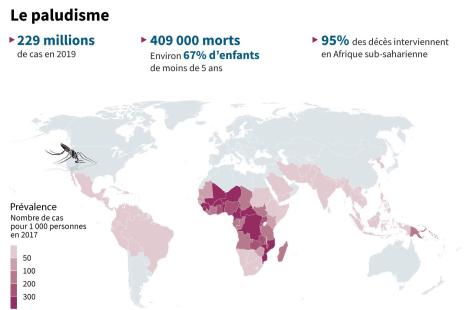
Le paludisme, qui demeure une endémie préoccupante, avec une incidence estimée par l’OMS (Organisation Mondiale de la Santé) à 241 millions de cas en 2020 et 627 000 décès, aurait donné lieu à 7 milliards de cas durant la période 2 000 – 2020 ainsi qu’à environ 10 millions de décès. Le premier responsable étant Plasmodium falciparum et l’Afrique la zone la plus touchée concentrant 94 % des cas de cette parasitose dans le monde.
De nombreux challenges à relever
Sujet de recherche mobilisant les chercheurs depuis plusieurs décennies, la mise au point de vaccins contre le paludisme se heurte à de multiples défis liés au mode de reproduction du parasite dont le cycle complexe se déroule chez deux hôtes (moustique et homme) ainsi qu’à la composition et à la variabilité de ses antigènes ; sans compter la difficulté à produire le ou les antigènes vaccinaux.
La mise au point de vaccins contre le paludisme se heurte à de multiples défis liés au mode de reproduction du parasite
Aujourd’hui, indique la Pr Odile Launay, la voie la plus explorée concerne le développement de vaccins subunitaires permettant d’induire une immunité efficace vis-à-vis de la forme pré-érythrocytaire de l’infection, dans le double objectif de protéger contre les formes sévères et aussi, en prévenant l’infection, d’interrompre la propagation du paludisme.
Un premier vaccin homologué
L’aventure du premier vaccin antipaludique ayant fait la preuve de son efficacité commence en 1984.
Développé par le laboratoire GSK, celui-ci commercialisé sous le nom de Mosquirix, renferme une protéine de surface recombinante de sporozoïte combinée à l’antigène HBs (AgHBs) produite dans la levure Saccharomyces cerevisiae. Ce vaccin (pseudo-particules virales immunogènes) renferme également un adjuvant (ASO1E).
Les tout premiers essais, qui débutent en 1995 chez quelques hommes volontaires, montrent une protection à hauteur de 85 % en cas d’infection par l’injection de sporozoïtes.
Suit en 1998 un essai clinique de phase II en zone d’endémie, en Gambie, impliquant environ 250 personnes qui permettent d’objectiver une protection à hauteur de 34 %.
Des candidats-vaccins de nouvelle génération sont actuellement en cours de développement, ciblant plusieurs stades du cycle parasitaire, testant de nouveaux adjuvants, mettant à profit les potentialités de l’ARN messager ou encore des vaccins vivants génétiquement atténués
Pr Odile Launay
Puis un grand essai de phase III qui débute en 2009 et aboutira à l’enregistrement de ce vaccin.
Ce dernier, randomisé contre placebo, va mobiliser 11 centres répartis dans 7 pays africains (Burkina Faso, Ghana, Gabon, Kenya, Tanzanie, Malawi et Mozambique), caractérisés par différentes intensités de transmission, et concerner 15 449 enfants (dont 6 527 nourrissons âgés de 6 à 12 semaines et 8 922 enfants entre 5 et 17 mois).
Les résultats montrent une plus grande efficacité chez les enfants vaccinés après l’âge de 5 mois et avec un schéma vaccinal comprenant 3 injections (J0, M1, M2) suivies d’un rappel à M20 : 36,3 % de protection contre les cas cliniques et de 32,2 % contre le paludisme sévère.
Au vu de ces données, l’Agence européenne du médicament émet un avis positif en juillet 2015.
En janvier 2016, l’OMS décide le lancement d’une nouvelle étude dans plusieurs pays africains avec 3 injections (J0, M1, M2) et un rappel à 15 – 18 mois chez des enfants âgés de 5 à 9 mois. Lancée à partir de 2019, cette étude a permis de vacciner plus de 830 000 enfants (2,4 millions de doses) au Kenya, Ghana et Malawi.
Les principales conclusions en sont une réduction importante des hospitalisations dues à une infection palustre, une baisse de 40 % du nombre d’épisodes cliniques et de 30 % des formes graves, de 13 % de la mortalité infantile (1 vie sauvée pour 200 enfants vaccinés), cela avec un impact vaccinal plus élevé dans les zones à forte endémie en vaccinant avant la saison des pluies (favorable à la multiplication des moustiques).
Le 6 octobre 2021, l’OMS recommande un déploiement à grande échelle du vaccin Mosquirix, en complément des autres moyens classiques de lutte (chimioprophylaxie, lutte antivectorielle), et le 22 janvier 2024 est lancée une première campagne nationale de vaccination au Cameroun.
Un second vaccin prometteur
Un autre vaccin adjuvanté (Matrix M), développé par le laboratoire Novavax, également subunitaire, pré-érythrocytaire et renfermant une protéine de sporozoïte associée à l’antigène HBs, a montré une efficacité de 77 % dans un essai de phase II mené en 2019 chez des enfants de 5 à 17 mois au Burkina Faso, suivi d’un essai de phase III (enfants de 5 à 36 mois, Burkina Faso, Mali, Kenya et Tanzanie), selon un schéma J0, M1, M2 + rappel à 1 an, ayant conforté ces données avec une protection de 75 % dans les zones à transmission saisonnière et de 68 % dans celles à transmission annuelle.
Enfin, conclut la Pr Odile Launay, « des candidats-vaccins de nouvelle génération sont en cours de développement, ciblant plusieurs stades du cycle parasitaire, testant de nouveaux adjuvants, mettant à profit les potentialités de l’ARN messager ou encore des vaccins vivants génétiquement atténués, sans oublier les technologies permettant la production à grande échelle des composants vaccinaux ».